
Подготовка и использование воды, умягченной натрий-катионитом, для заправки систем охлаждения двигателей
Вода, умягченная методом натрий-катионирования, при нагревании приобретает щелочную среду. Такая вода непригодна для двигателей с алюминиевыми блоками или головками цилиндров, так как алюминии сильно корродирует в щелочной среде. Поэтому прежде чем использовать эту воду, необходимо устранить ее щелочность нейтрализацией какой-либо кислотой (серной, соляной, фосфорной, хромовой). t
Объем кислоты, необходимый для устранения щелочности умягченной воды, можно вычислить по карбонатной жесткости воды Жк согласно уравнению
Vк = 100ЖкЭкVн/Pd (2)
а весовое количество кислоты -по уравнению
mк = ЭкЖкVн,
где
Vк - объем кислоты, прибавляемой к воде, мл;
Жк - карбонатная жесткость воды, гэкв/м ;
Эк - эквивалент кислоты; .
Vн - объем нейтрализуемой умягченной воды, м;
Р - процентное содержание кислоты в исходном продукте;
d - плотность исходной кислоты, г/мл;
mк - вес кислоты, добавляемой к воде, г.
Пример. Пусть в емкости находится 15 м3 умягченной воды, в которой содержание бикарбонатов равно 2,5 мгэкв/л (2,5 гэкв/м). Количество концентрированной 96-процентной серной кислоты (плотность 1,84, эквивалент - 49), которое следует добавить, будет равно
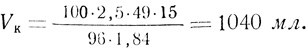
С одинаковым успехом можно применять соляную, фосфорную и хромовую кислоты, количество которых можно вычислить по уравнению (2). Их плотность и концентрацию в исходных товарных продуктах можно найти в справочнике по химии.
Получение нейтральной воды на практике довольно сложный процесс, так как трудно с достаточной точностью замерить объем воды в емкости и отмерить объем кислоты. Поэтому необходимо, чтобы емкость для умягченной воды была прокалибрована возможно точнее, кислоту следует брать не концентрированную, а разбавленную, но с точно измеренной концентрацией и плотностью. Воду с кислотой необходимо тщательно перемешивать паром или сжатым и нагретым воздухом при помощи инжектора, установленного в днище емкости.
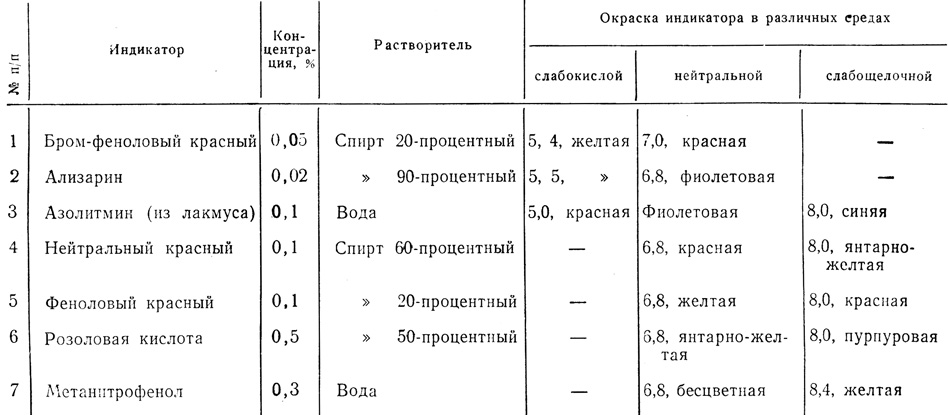
Таблица 4. Таблица индикаторов с интервалом перехода в среде, близкой к нейтральной
Примечание. Цифры в графах "Окраска индикатора в различных средах" показывают величину водородного показателя pH, при котором индикатор имеет окраску, указанную в тех же графах.
После перемешивания воду проверяют индикатором, который практически точно показывает нейтральную среду. При этом вода может оказаться слабощелочной или слабокислотной. Это обстоятельство вызывает необходимость в корректировке среды воды. Если количество кислоты, прибавленной к воде, недостаточно, то реакция - слабощелочная. В этом случае следует прибавлять кислоту малыми порциями при энергичном размешивании до тех пор, пока пробы воды с одним из индикаторов (№ 3-№ 7), приведенных в табл. 4, не покажут окраску, соответствующую нейтральной среде. Такую корректировку воды можно провести и на основании ее анализа. Так как остаточное содержание бикарбонатов невелико, то их определяют титрованием проб воды из микробюретки 0,05 н-раствором кислоты. В качестве индикатора можно рекомендовать раствор розоловой кислоты. Количество воды для одного титрования следует подобрать опытным путем. Количество кислоты Vк, необходимое для корректировки среды воды, можно найти, пользуясь уравнением (2), где вместо величины жесткости Жк следует взять остаточную концентрацию бикарбоната. 26
Если количество прибавленной кислоты окажется большим и вода будет иметь слабокислую среду, тогда к воде можно добавить уксуснокислый .натрий, буру или хромпик в таком количестве, чтобы пробы воды с одним из индикаторов № 1-№ 3 табл. 4 показали окраску, соответствующую нейтральной среде.
Количество той или другой соли можно рассчитать по уравнению
mс = КЭсV,
где mс - количество соли, прибавляемой к воде, г;
К - избыточная концентрация кислоты, мгэкв/л (или гэкв/м3);
Эс - эквивалент соли;
V - объем воды, м3.
Эквивалент кристаллического уксуснокислого натрия СН3СОONa*3Н2O равен 136,09; кристаллической буры Na2B4O7*10H2O - 190,72, а хромпика К2Cr2O7 - 147,1.
Умягченная вода содержит в растворенном состоянии кислород, который вызывает коррозию стенок котлов и систем охлаждения двигателей. При полном умягчении воды до 0,03 мгэкв/л на стенках емкости, в которой вода нагревается, слой накипи будет отсутствовать, что будет способствовать коррозии. Поэтому рекомендуется не доводить жесткость умягченной воды до минимальной величины, а поддерживать ее близкой к 0,2 мгэкв/л. При этом на стенках емкости будет создаваться тончайший слой накипи, который предохранит стенки от коррозии. Если фильтр дает очень мягкую воду, то к ней рекомендуют добавлять определенное количество неумягченной воды, доводя общую жесткость смешанной воды до 0,2 мгэкв/л.
Количество добавляемой неумягченной воды можно определить, пользуясь следующим уравнением:
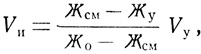
где Vи - объем неумягченной воды, добавляемой к умягченной, м3;
Vy - объем умягченной воды, м3;
Жv - общая остаточная жесткость умягченной воды, гэкв/м3;
Ж0 - общая жесткость неумягченной воды, гэкв/м3;
Жсм - общая жесткость воды после смешивания, гэкв/м3.
Пример. Определим необходимое количество неумягченной воды, добавляемой к умягченной. Пусть в емкости находится 15 м3 умягченной воды с остаточной жесткостью 0,05 гэкв/м3. Общая жесткость неумягченной воды составляет 10 гэкв/м3. Требуется найти объем неумягченной воды, которую надо добавить, чтобы после смешения с умягченной жесткость была равной 0,2 гэкв/м3. Подбавляя значения величин в вышеприведенное уравнение, получим
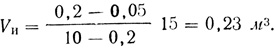
Таким образом, если к 15 м3 умягченной воды с остаточной жесткостью 0,05 гэкв/м3 прибавить 0,23 м3 неумягченной воды с жесткостью 10 гэкв/м3, то полученная смешанная вода будет иметь жесткость Жсм = 0,2 гэкв/м3.
Умягчение воды, ее анализ на щелочность, расчет количества химикатов, нейтрализация, перемешивание и, наконец, подогрев должны быть проведены заранее до начала заправки систем охлаждения двигателей водой перед выездом на линию. Очевидно, время tпод, необходимое для полной подготовки воды, будет равно
tпод = ty + tx + tн + tп,
где ty - время, затрачиваемое на умягчение воды в количестве, обеспечивающем заправку всех двигателей, ч;
tх - время, необходимое для анализа воды и расчета добавки химикатов, ч;
tн - время для нейтрализации и перемешивания, ч;
tп - время на подогрев воды, ч.
Значения всех этих величин зависят от условий работы каждого автотранспортного предприятия. Можно рекомендовать все операции проводить в течение одной смены, а подогрев воды-непосредственно перед заправкой двигателей перед выездом на линию.
|
ПОИСК:
|
© MOTORZLIB.RU, 2001-2020
При использовании материалов сайта активная ссылка обязательна:
http://motorzlib.ru/ 'Автомобилестроение, наземный транспорт и организация движения'
При использовании материалов сайта активная ссылка обязательна:
http://motorzlib.ru/ 'Автомобилестроение, наземный транспорт и организация движения'